Mette in risalto
-
Identificazione di immunocorrelati in un caso di epatite autoimmune associata al vaccino mRNA
-
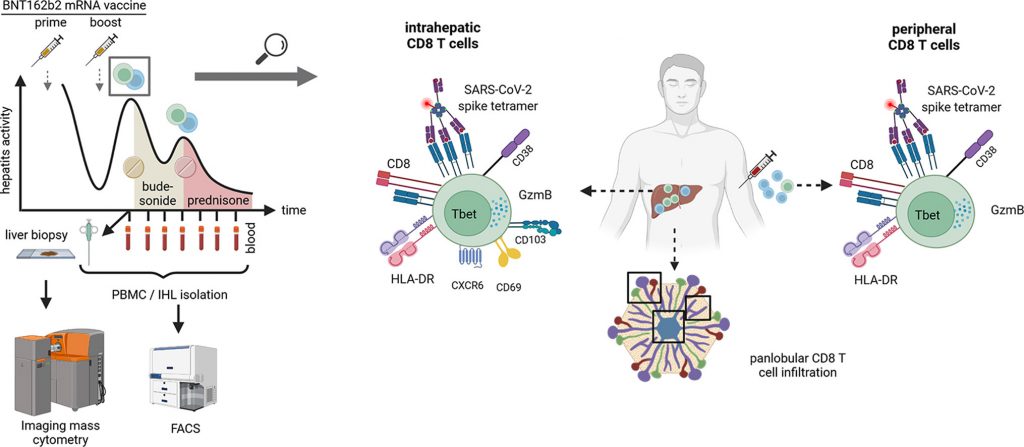
La citometria di massa per immagini identifica l’arricchimento panlobulare intraepatico delle cellule T CD8 citotossiche attivate
-
La citometria a flusso identifica l’arricchimento intraepatico delle cellule T CD8 attivate con specificità SARS-CoV-2
-
L’attivazione delle cellule T CD8 specifiche per SARS-CoV-2 periferica è correlata ai livelli di ALT
Astratto
Sfondo e obiettivi
Metodi
Risultati
Conclusioni
Riepilogo laico
Introduzione
La vaccinazione è la strategia chiave per combattere la pandemia globale di COVID19. Non c’era alcun segnale di sicurezza per l’epatite negli studi di vaccinazione COVID19 [1]. Tuttavia diversi rapporti hanno recentemente associato condizioni simili all’epatite autoimmune (AIH) con i vaccini COVID19 [[2 3 4 5 6 7 8 9 10 11].
A nostra conoscenza, non è stato segnalato alcun caso grave di insufficienza epatica che richieda il trapianto di fegato. Il danno epatico è stato osservato dopo entrambi i vaccini a base di mRNA e vettori, mentre il tempo dalla somministrazione del vaccino all’insorgenza dei sintomi variava da 4 giorni dopo la prima dose a 6 settimane dopo la seconda dose. Un paziente è stato riesposto al vaccino che ha portato a un peggioramento del danno epatico [11].
Non è chiaro se l’associazione segnalata dell’epatite autoimmune con la vaccinazione sia casuale, potrebbe riflettere un danno epatico transitorio indotto da farmaci o potrebbe implicare un’attivazione immunitaria specifica dell’antigene indotta da SARS-CoV-2. [12]
Tuttavia, il fatto che condizioni simili all’AIH si siano verificate anche dopo l’infezione da SARS-CoV-2 [13] suggerisce che quest’ultimo potrebbe essere un fattore trainante per i casi sporadici.
Decorso clinico
Il paziente di sesso maschile di 52 anni senza una storia medica degna di nota a parte l’ipotiroidismo preesistente in terapia sostitutiva a lungo termine con levotiroxina e test di funzionalità epatica normale (LFT) ha sviluppato nausea progressiva, affaticamento, perdita di appetito e prurito con sintomi che iniziano circa 10 giorni dopo la prima dose (prime) del vaccino mRNA BNT162b2. Successivamente ha sviluppato ittero e si è presentato al suo medico di base con LFT indicativo di epatite acuta mista epatocellulare/colestatica (ALT: 2130 U/l, AP: 142 U/l gamma-GT: 217 U/l, Bilirubina 7,7 mg/dl) ( Fig. 1). Il paziente è stato ricoverato in un centro di cure primarie 25 giorni dopo la prima vaccinazione. L’epatite virale A, B, C ed E così come le infezioni da citomegalovirus e virus di Epstein-Barr sono state escluse dalla sierologia e/o dal test PCR. La genotipizzazione HFE non ha rivelato variazioni associate all’emocromatosi. Inoltre, non è stato riscontrato alcun consumo significativo di alcol e la sierologia autoimmune è rimasta inconcludente con la reattività borderline AMA-M2. Il paziente si è ripreso rapidamente senza una terapia specifica ed è stato dimesso con LFT in diminuzione dopo tre giorni sotto la diagnosi differenziale principale di un’epatite tossica. Nelle due settimane successive, gli enzimi epatici sono ulteriormente diminuiti, con la normalizzazione di AST e AP e il paziente ha ricevuto la sua seconda dose (boost) del vaccino mRNA BNT162b2 41 giorni dopo la prima vaccinazione ( Fig. 1). 20 giorni dopo la vaccinazione boost (dpb), il paziente ha rivissuto nausea e affaticamento. I test di laboratorio hanno rivelato una ricaduta di epatite mista acuta con (ALT 1939 U/l, ALP 167 U/l, bilirubina 2,9 mg/dl). Successivamente è stato indirizzato al nostro centro terziario a 26 dpb. La sierologia autoimmune è stata ripetuta con lieve iperglobulinemia (livelli di IgG 1,02 volte rispetto all’ULN, livelli normali di IgA e IgM), ANA (1:200) e positività borderline per anticorpi anti-muscolo liscio e AMA-M2 mentre i test per anti-LKM sono rimasti negativi . Abbiamo eseguito una biopsia epatica che istologicamente ha mostrato epatite di interfaccia con un grado moderato di infiltrato linfoplasmocitico e focolai di necrosi lobulare e apoptosi. Non erano presenti granulociti eosinofili. Non sono state osservate fibrosi perisinusoidale né portale rilevanti. Insieme [14] e il paziente è stato trattato con 9 mg di budesonide orale al giorno. Nelle settimane successive gli enzimi epatici sono diminuiti prima che si verificasse una ricaduta 39 giorni dopo l’inizio della terapia (66 dpb), che è stata controllata successivamente dopo l’escalation della terapia con steroidi sistemici in combinazione con acido ursodesossicolico. Gli LFT del paziente si sono successivamente normalizzati entro 8 settimane ( Fig. 1 ). Gli anticorpi anti-spike non hanno mostrato fluttuazioni maggiori con titoli simili rispetto agli individui sani al momento della diagnosi a 27 giorni dopo la vaccinazione boost ( Fig. 1 B) e una riduzione prevista dei titoli nel tempo ( Fig 1 C).
Risultati
Analisi immunitaria spaziale profonda del tessuto epatico
Immunofenotipizzazione periferica intraepatica e longitudinale delle risposte delle cellule T CD8 associate alla vaccinazione
Discussione
È quindi importante differenziare l’AIH dall’epatite immuno-mediata possibilmente transitoria dopo la vaccinazione. La diagnosi di epatite autoimmune viene in genere stabilita utilizzando strumenti di punteggio AIH basati su test di funzionalità epatica, sierologia autoanticorpale e caratteristiche istologiche tipiche come l’epatite dell’interfaccia e l’arricchimento delle plasmacellule [14]. Nel nostro caso, prima della terapia, la diagnosi di AIH era considerata “probabile” sulla base del punteggio AIH originale modificato. È importante notare in questo contesto che il primo episodio di epatite acuta dopo la prima dose di vaccino è stato autolimitante senza terapia, il che ha anche guidato la nostra scelta di iniziare la terapia con budesonide nel tentativo di ridurre al minimo gli effetti collaterali sistemici e di mantenere anti- -Immunità SARS-Cov2 se possibile. Tuttavia, il nostro paziente ha avuto una ricaduta 3-4 settimane dopo la terapia con budesonide e quindi ha richiesto una terapia steroidea sistemica, che è stata empiricamente combinata con acido ursodesossicolico, una combinazione utilizzata nella terapia della sindrome da sovrapposizione di epatite autoimmune che è stata scelta per la presenza di AMA-M2 anticorpi che si trovano tipicamente nella colangite biliare primitiva [17]. Il paziente si è successivamente ripreso rapidamente, con solo una gengivite che si è verificata durante la terapia steroidea sistemica come possibile evento correlato all’immunosoppressione. A causa della recidiva dell’epatite dopo la riduzione graduale degli steroidi, il paziente è stato sottoposto a terapia immunosoppressiva di mantenimento a lungo termine in base alla quale ha ottenuto una completa remissione biochimica.
Metodi
Campioni di pazienti
Citometria di massa per immagini
In breve, dopo la deparaffinazione, la reidratazione, il recupero dell’antigene e il blocco, i vetrini sono stati colorati con anticorpi marcati con metallo ed essiccati all’aria. L’acquisizione dell’immagine della biopsia (30,912 mm 2 ) e 2,25 mm 2 dei campioni di controllo è stata eseguita utilizzando un sistema di imaging Hyperion (Fluidigm; USA). Le ROI sono state asportate al laser punto per punto a 200 Hz, ottenendo una risoluzione in pixel di 1 μm 2. La visualizzazione delle immagini è stata eseguita con FIJI (v1.52p, ImageJ). La segmentazione delle singole celle è stata condotta utilizzando una pipeline di analisi supervisionata e imparziale adattata utilizzando Ilastik (v 1.3.3) e CellProfiler (v 3.1.9). Per analizzare le zone del fegato, la distanza di ciascun pixel da GLUL, CD34 e α-SMA è stata calcolata utilizzando CellProfiler (v 4.0.4), aggiunto alle informazioni ad alta dimensione di ciascuna cellula e utilizzato per il gating in OMIQ (Omiq Inc). Le zone epatiche sono state definite: centrolobulare (distanza da GLUL ≤50 μm), periportale (distanza da GLUL >50 μm e distanza da CD34 e α-SMA ≤50 μm) e intermedie (distanza da GLUL >50 μm e distanza da CD34 e α- SMA >50 μm). La conta cellulare assoluta è stata normalizzata a 1 mm 2 . I grafici a barre in pila sono stati creati con la versione R 4.0.1 utilizzando ggplot2.
Isolamento PBMC
Sospensione unicellulare da biopsia epatica
Analisi di cellule T CD8+ specifiche per spike
Citometria a flusso multiparametrica
Riduzione dimensionale dei dati di citometria a flusso multiparametrica
ELISA
Dichiarazione di disponibilità dei dati
I set di dati generati dalla citometria a flusso e dalla citometria di massa per imaging saranno resi disponibili in conformità con le normative legali su richiesta ragionevole.
Fonti di finanziamento
Il lavoro è stato sostenuto da sovvenzioni del Ministero federale tedesco dell’istruzione e della ricerca (01KI2077 per MH e RT) e della Fondazione tedesca per la ricerca (272983813 per BB, TB, RT, MH e CNH; 256073931 per BB, RT, MH e CNH ; 413517907 a HL, 378189018 a BB). HL e MS sono supportati dal programma IMM-PACT per scienziati clinici, Dipartimento di Medicina II, Centro medico – Università di Friburgo e Facoltà di Medicina, Università di Friburgo, finanziato dalla Deutsche Forschungsgemeinschaft (DFG, Fondazione tedesca per la ricerca) – 413517907 .TB e SM sono supportati dal programma Berta-Ottenstein per scienziati clinici, Facoltà di Medicina, Università di Friburgo. Il lavoro di MH è ulteriormente supportato dalla borsa di studio Margarete von Wrangell (Stato del Baden-Wuerttemberg).
Dichiarazione di conflitto di interessi
Contributi degli autori
Ideazione e progettazione dello studio (TB, MH, BB); esperimenti e procedure (BC, HS, HL, LW, ESA, KZ, LK, MS); reclutamento di campioni di pazienti (TB, BB), valutazione istologica (CM,PB), analisi bioinformatica e statistica (BC, HS, HL, ESA); interpretazione dei dati e stesura del manoscritto (TB, MH, BB); revisione del manoscritto per importanti contenuti intellettuali (MP, CNH, RT);
Ringraziamenti
Ringraziamo la paziente per la donazione di campioni e Saskia Killmer e Marilyn Salvat Lago della struttura di citometria di massa di Friburgo per l’eccellente servizio tecnico.
Appendice A. Dati supplementari
I seguenti sono/sono i dati supplementari a questo articolo.
Riferimenti
- Polacco FP
- Thomas SJ
- Kitchin N.
- Absalon J.
- Gurtman A.
- Lockhart S.
- et al.
Sicurezza ed efficacia del vaccino BNT162b2 mRNA Covid-19.Giornale di medicina del New England. 2020; 383 : 2603-2615Palla P, Vergadis C, Sakellariou S, Androutsakos T. Lettera all’editore: epatite autoimmune dopo la vaccinazione COVID-19. Un raro effetto negativo? Epatologia;n/a.
- Bril F.
- Al Difalha S.
- Dean M.
- Fetti DM
Epatite autoimmune in via di sviluppo dopo il vaccino contro la malattia di coronavirus 2019 (COVID-19): causalità o incidente?.Giornale di epatologia. 2021; 75 : 222-224- Clayton-Chubb D.
- Schneider D.
- Freeman E.
- Kemp W.
- Roberts SK
Commento alla lettera di Bril F et al. “Epatite autoimmune in via di sviluppo dopo il vaccino contro la malattia di coronavirus 2019 (COVID-19): causalità o incidente?”.Giornale di epatologia. 2021;- Lodato F.
- Larocca A.
- D’Errico A.
- Cennamo V.
Un caso anomalo di epatite colestatica acuta dopo il vaccino m-RNA BNT162b2 (Comirnaty) SARS-CoV-2: coincidenza, autoimmunità o danno epatico correlato a farmaci?.Giornale di epatologia. 2021;- Londoño M.-C.
- Gratacos-Ginès J.
- Sáez-Peñataro J.
Un altro caso di epatite autoimmune dopo la vaccinazione SARS-CoV-2. Ancora vittima?.Giornale di epatologia. 2021;- McShane C.
- Kiat C.
- Rigby J.
- Crosbie O.
Il vaccino mRNA COVID-19 – un raro fattore scatenante dell’epatite autoimmune?.Giornale di epatologia. 2021;- Rocco A.
- Sgamato C.
- Rispetto.
- Nardone G.
Epatite autoimmune dopo il vaccino SARS-CoV-2: potrebbe non essere una casualità.Giornale di epatologia. 2021;- Shroff H.
- Satapatia SK
- Crawford JM
- Todd NJ
- Van Wagner LB
Danno epatico a seguito della vaccinazione SARS-CoV-2: una serie di casi multicentrici.Giornale di epatologia. 2021;- Tan CK
- Wong YJ
- Wang LM
- Ang TL
- Kumar R.
Epatite autoimmune a seguito di vaccinazione COVID-19: vera causalità o mera associazione?.Giornale di epatologia. 2021;- Tu GSZ
- Gleson D.
- Dube A.
- Al-Joudeh A.
Epatite immuno-mediata con il vaccino Moderna, non più una coincidenza ma confermata.Giornale di epatologia. 2021;- Fernando B.
Epatite autoimmune in via di sviluppo dopo il vaccino contro la malattia di coronavirus 2019 (COVID-19): una o anche più rondini non fanno estate.Giornale di epatologia. 2021;- Kabaçam G.
- Wahlin S.
- Efe C.
Epatite autoimmune innescata da COVID-19: una relazione di due casi.Internazionale del fegato. 2021; 41 : 2527-2528- Alvarez F.
- Berg PA
- Bianchi FB
- Bianchi L.
- Burroughs AK
- Canado EL
- et al.
Rapporto del gruppo internazionale sull’epatite autoimmune: revisione dei criteri per la diagnosi di epatite autoimmune.Giornale di epatologia. 1999; 31 : 929-938- Oberhardt V.
- Luxenburger H.
- Kemming J.
- Schulien I.
- Ciminski K.
- Giese S.
- et al.
Mobilitazione rapida e stabile delle cellule T CD8+ da parte del vaccino mRNA SARS-CoV-2.Natura. 2021;- Linee guida EASL per la pratica clinica
Epatite autoimmune.Giornale di epatologia. 2015; 63 : 971-1004- Younossi ZM
- Bernstein D.
- Shiffman ML
- Kwo P.
- Kim WR
- Kowdley KV
- et al.
Diagnosi e gestione della colangite biliare primitiva.La rivista americana di gastroenterologia. 2019; 114 : 48-63- Mehal WZ
- Juedes AE
- Croccante IN
Ritenzione selettiva di cellule T CD8+ attivate da parte del fegato normale.J Immunol. 1999; 163 : 3202-3210- Belz GT
- Altman JD
- PC di Doherty
Caratteristiche delle cellule T CD8(+) virus-specifiche nel fegato durante le fasi di controllo e risoluzione della polmonite influenzale.Proc Natl Acad Sci US A. 1998; 95 : 13812-13817- Bowen DG
- Warren A.
- Davis T.
- Hoffmann MW
- McCaughan GW
- Fazekas de St Groth B.
- et al.
Epatite da spettatore dipendente da citochine dovuta all’attivazione intraepatica dei linfociti T CD8 murini da parte di cellule derivate dal midollo osseo.Gastroenterologia. 2002; 123 : 1252-1264- Kim J.
- Chang DY
- Lee HW
- Lee H.
- Kim JH
- Cantato PS
- et al.
La funzione citotossica innata delle cellule T CD8(+) attivate da un astante è associata a lesioni epatiche nell’epatite acuta A.Immunità. 2018; 48 ( e165 ) : 161-173- Sandalova E.
- Laccabue D.
- Boni C.
- Abbronzatura AT
- Fink K.
- Ooi EE
- et al.
Contributo delle cellule T CD8 specifiche dell’herpesvirus alla risposta antivirale delle cellule T nell’uomo.PLoS Pathog. 2010; 6 e1001051- Dudek M.
- Pfister D.
- Donakonda S.
- Filpe P.
- Schneider A.
- Laschinger M.
- et al.
Le cellule T CD8 CXCR6(+) auto-aggressive causano la patologia immunitaria del fegato nella NASH.Natura. 2021; 592 : 444-449- Pfister D.
- Nunez NG
- Pinyol R.
- Govaere O.
- Pinter M.
- Szydlowska M.
- et al.
La NASH limita la sorveglianza antitumorale nell’HCC trattato con immunoterapia.Natura. 2021; 592 : 450-456- Schwabenland M.
- Salié H.
- Tanevski J.
- Killmer S.
- Lago MS
- Schlaak AE
- et al.
La profilazione spaziale profonda del cervello umano COVID-19 rivela la neuroinfiammazione con interazioni microanatomiche distinte della microglia-cellule T.Immunità. 2021; 54 ( e1511 ) : 1594-1610
Informazioni sull'articolo
Storia della pubblicazione
Fase di pubblicazione
In Press Journal Pre-ProofIdentificazione
Diritto d’autore
ScienceDirect
Accedi a questo articolo su ScienceDirectArticoli correlati
- Bassa immunogenicità alla vaccinazione SARS-CoV-2 tra i riceventi di trapianto di fegatoRabinowich et al.Giornale di epatologia20 aprile 2021
- Aumenti inspiegabili del test del fegato dopo la vaccinazione SARS-CoV-2Guardiola et al.Giornale di epatologia10 marzo 2022
- Infezione da SARS-CoV-2 in pazienti con epatite autoimmuneMarjot et al.Giornale di epatologia25 gennaio 2021Accesso libero
- Efficacia della vaccinazione SARS-CoV-2 nei pazienti trapiantati di fegato: il dibattito è aperto!Guarino et al.Giornale di epatologia3 agosto 2021
- Un altro caso di epatite autoimmune dopo la vaccinazione SARS-CoV-2 – ancora vittima?Londono et al.Giornale di epatologia12 giugno 2021